ブレインクラフトのウェブサイトへようこそ!
当社は医療機器の設計開発から許認可申請に係るコンサルタント会社です。また、カナダで開発された高性能な家庭用大気汚染対策マスクO2 Curve(オーツーカーブ)の国内で唯一の正規輸入元です。
O2 Curve(オーツーカーブ) 高性能マスク 公式オンラインショップ
シリコンで密着させ、フィルターでろ過するマスク。守られている安心感を!
カナダで開発された高性能な家庭用大気汚染対策マスク『O2 Curve』(オーツーカーブ)。医療用シリコンで顔面にしっかりと密着させ、内部のフィルターを交換するタイプの繰り返し使えるマスクです。0.1ミクロン以上の粒子を効率的にろ過し、あなたの体を守ります。
ハウスダストが気になる方、受験生の方にオススメです!
#マスク #ハウスダスト #対策 #グッズ #受験生 #応援 #試してみた #お守り

O2カーブは Amazon でもご購入いただけます。


#O2カーブ #O2Curve #マスク #ハウスダスト #対策 #グッズ #受験生 #応援 #試してみた #ホコリ#N95 #コロナ #サバゲー #迷彩 #ヒョウ柄 #立体 #密着 #医療 #フィット #シリコン #防じん #ウイルス #高性能 #呼気弁 #フィルター #快適 #3D #三次元 #感染予防 #花粉症 #サージカル #風邪 #インフルエンザ #介護 #ブレインクラフト #黄砂 #火山灰 #自転車 #PM2.5 #塗装 #タクシー #バス
普段のマスクに加えて
「お守りマスク=O2カーブ」を持ち歩こう!
病院や劇場、公共の乗り物など、密になる空間ではとても心配!
そんな時、普段のマスクに加えて「O2カーブ」を一つ持っていると安心です。
ご自身のために、そして大切な方への贈り物に♡
#マスク #ハウスダスト #対策 #グッズ #受験生 #応援 #試してみた #お守り
#O2カーブ #O2Curve #マスク #ハウスダスト #対策 #グッズ #受験生 #応援 #試してみた #ホコリ#N95 #コロナ #サバゲー #迷彩 #ヒョウ柄 #立体 #密着 #医療 #フィット #シリコン #防じん #ウイルス #高性能 #呼気弁 #フィルター #快適 #3D #三次元 #感染予防 #花粉症 #サージカル #風邪 #インフルエンザ #介護 #ブレインクラフト #黄砂 #火山灰 #自転車 #PM2.5 #塗装 #タクシー #バス
O2カーブ マスク本体

O2カーブ・マスク本体セット(+2weekフィルター3枚付属)


#O2カーブ #O2Curve #マスク #ハウスダスト #対策 #グッズ #受験生 #応援 #試してみた #ホコリ#N95 #コロナ #サバゲー #迷彩 #ヒョウ柄 #立体 #密着 #医療 #フィット #シリコン #防じん #ウイルス #高性能 #呼気弁 #フィルター #快適 #3D #三次元 #感染予防 #花粉症 #サージカル #風邪 #インフルエンザ #介護 #ブレインクラフト #黄砂 #火山灰 #自転車 #PM2.5 #塗装 #タクシー #バス
O2カーブ 交換フィルター
『O2 Curve(オーツーカーブ)』交換フィルターのご紹介
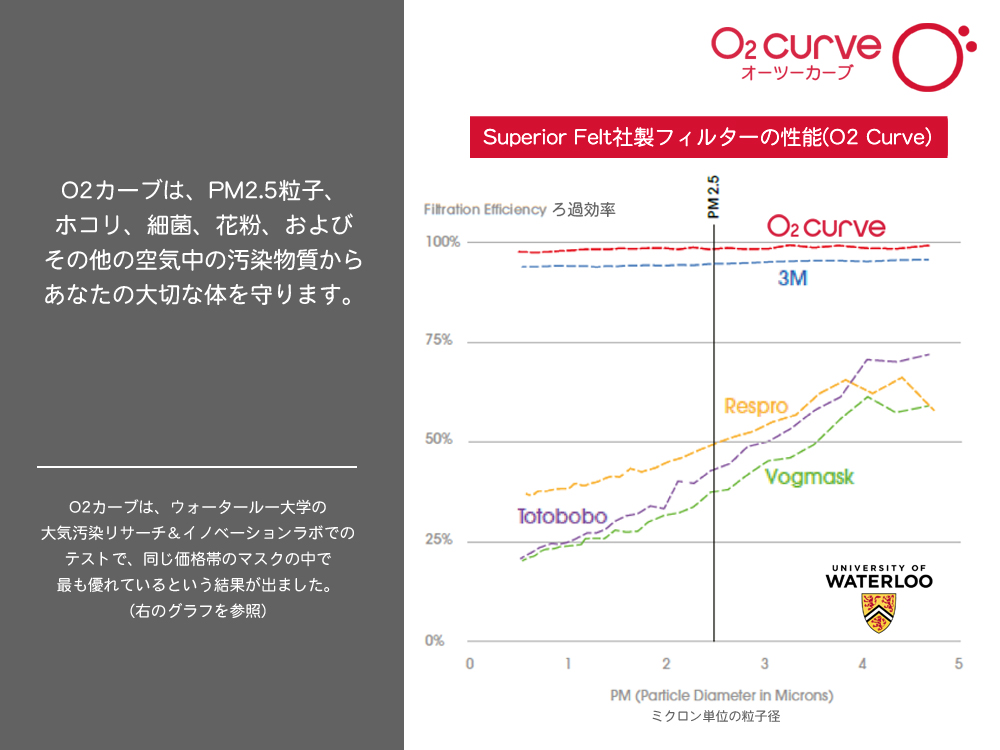
O2カーブの静電フィルターは、0.1ミクロン以上の粒子を効率的にろ過します。マイナス(-)とプラス(+)の両方に帯電したポケットで小さな粒子を引きつけ中和させることで、空気中の機械的汚染物質だけでなく、バクテリアや病原菌にも非常に効果的です

O2カーブで使用されているフィルターは、米国最大級の在庫を誇るSuperior Felt & Filtration社製です。
マスクは二重にするよりも、隙間をなくす方が効果的とのことです。
O2カーブ 交換シェル
気分に合わせて着替えよう!『O2 Curve(オーツーカーブ)』交換シェルのご紹介
O2カーブ 価格表


O2カーブは Amazon でもご購入いただけます。